natuurkunde
Foto-elektrisch effect
Deze applet behandelt het foto-elektrisch effect.
om de applet te starten
(in een nieuw scherm).
(in een nieuw scherm).
Applet: The King's Centre for Visualisation in Science (The King's University, Canada)
https://kcvs.ca
https://kcvs.ca
Het foto-elektrisch effect
Elektromagnetische straling kan de elektronen uit een metaal, die niet zo sterk gebonden zijn aan een atoom, vrij maken. Dat is eind 19e eeuw ontdekt en wordt sindsdien het foto-elektrisch effect genoemd, ook wel foto-emissie.Aantonen van het foto-elektrisch effect
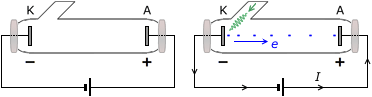
In een vacuüm buis zijn twee elektroden aangebracht. Je sluit de elektroden aan op een spanningsbron, waardoor de ene elektrode positief wordt (A: de anode), en de andere negatief (K: de kathode). Ondanks de spanning loopt er geen elektrische stroom, want er is geen gesloten kring.Als je nu de kathode bestraalt met elektromagnetische straling met een frequentie die hoog genoeg is, dan loopt er tóch elektrische stroom.
Met de energie van de straling kunnen elektronen uit het metaal van de kathode ontsnappen. De ontsnapte elektronen worden door de anode aangetrokken en stromen door naar de pluspool van de spanningsbron. De minpool vult de elektronen in de kathode aan en de stroomkring is compleet. Zie de figuur.
Grensfrequentie
Elk metaal blijkt zijn eigen grensfrequentie te hebben. Alleen elektromagnetische straling met een frequentie boven deze grens kan foto-emissie veroorzaken. Straling met een frequentie onder de grensfrequentie nooit, hoe intens (fel) de straling ook is.Verklaring van het foto-elektrisch effect
- Uittree-energie
In metalen zijn sommige elektronen niet zo sterk aan een atoomkern gebonden. Als je een metalen voorwerp (bijvoorbeeld de kathode) voldoende stralingsenergie aanbiedt, kan zo'n zwak gebonden elektron 'uittreden': uit het metaalrooster ontsnappen. De kleinste hoeveelheid energie die daar per elektron voor nodig is noem je de uittree-energie (Euit). - Fotonen
Om de grensfrequentie te begrijpen heb je het deeltjesmodel van straling nodig. Volgens dit model bestaat elektromagnetische straling uit fotonen. Dat zijn stralingsdeeltjes, kleine 'pakketjes' stralingsenergie, elk met een energie Efoton = h·f, met h de constante van Planck en f de frequentie van de straling. - Het foto-elektrisch effect
De grensfrequentie begrijp je nu met deze aanname:Elk elektron kan de stralingsenergie van slechts één foton tegelijk benutten.- Is de frequentie fstraling van de straling kleiner dan de grensfrequentie fgrens van het metaal, dan geldt voor alle fotonen: Efoton < Euit , dus kan geen enkel elektron ontsnappen. Geen foto-emissie dus, hoe intens de straling ook is.
- Is fstraling gelijk aan fgrens , dan geldt voor alle fotonen: Efoton = Euit en kan een elektron, na absorptie van de energie, ontsnappen.
- Is fstraling groter dan fgrens , dan houdt een elektron na ontsnapping zelfs nog wat kinetische energie over.
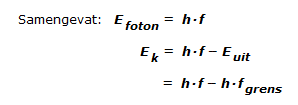
De applet
Na het titelscherm zie je een vacuüm buis met links de kathode en rechts de anode. De kathode wordt bestraald met fotonen.- Links onder regel je de intensiteit van de straling.
- Onder 'Options' kies je het metaal van de kathode. Standaard is dat natrium (sodium).
- Links van het spectrum typ je de golfengte van de straling. Bevestig je keuze met enter of door in het spectrum te klikken. Rechts zie je dan de frequentie.
- Ga na dat er slechts foto-emissie is als de frequentie van de straling groter is dan de grensfrequentie van het kathodemetaal.